
Исследование проблемы в социальном и историческом контексте
Исторические сценарии и эволюция инструментов фиксации
Изучение связи «приём препарата — самочувствие» требует погружения в историю вопроса: как люди в разные эпохи и в разных условиях фиксировали информацию о лечении и самочувствии, какие артефакты и практики для этого существовали. Это историко-культурное рассмотрение позволяет понять предпосылки текущих проблем.
Рис. X. The War: Wounded Servians in the Hospital at Usicza. Гравюра. Неизвестный автор. XIX век.
До 1950-х годов: домашние заметки и фармакопеи. В допечатный период и вплоть до середины XX века фиксация приёма лекарств велась преимущественно в домашнем и фармакопейном формате. Артефакты того времени — личные тетради, куда записывали назначенные лекарства и наблюдения за больным, семейные «больничные журналы», которыми пользовались при уходе на дому, ярлыки на аптечных склянках с краткими указаниями. Национальные фармакопеи и лечебники, издаваемые ограниченным тиражом, служили справочниками, но не интерактивными дневниками.

Разворот одного из томов медицинских клинических журналов, XVII в.
Социальные факторы этой эпохи заключались в том, что забота о больных распределялась внутри семьи: несколько родственников могли по очереди давать лекарства, и чтобы избежать ошибок, делали общую тетрадь наблюдений. Экономические факторы тоже играли роль: лекарства были дорогими и не всегда доступными, поэтому фиксировали расход лекарств и наличие запаса — это было сродни бухгалтерскому учёту, чтобы не потратить лишнего и вовремя пополнить аптечку. Политико-правовая среда характеризовалась ограниченной доступностью врачей и формальных инструкций: врачебные назначения часто ограничивались устным советом или краткой запиской на латыни, непонятной пациенту. Поэтому семьи переписывали схему лечения в «бытовой» форме, понятными словами, дополняли собственными пометками о том, как реагирует больной.
Ключевым событием середины XX века можно назвать начало стандартизации аптечных этикеток с указанием режима дозирования. По мере индустриализации фармации стала нормой печать на этикетке понятных инструкций («принимать по 1 таблетке 3 раза в день после еды» и т. п.), что снизило необходимость переписывать назначения вручную. Тем не менее, в целом до 1950-х годов учёт приёма препаратов вёлся преимущественно «для памяти семьи», а не для отчётности врачу. Врач при встрече полагался на устный рассказ пациента о том, что он принимал и как себя чувствовал.


Слева: Этикетка лекарства, 1937 г. Справа стандартизированная этикетка лекарства, 1990-е г.
1950–1980-е: клинические бумажные дневники и первые упаковочные решения. В послевоенные десятилетия произошёл заметный сдвиг в способах фиксации лечения, обусловленный ростом хронических терапий и развитием контроля безопасности лекарств. Артефакты этого периода включают бумажные дневники симптомов (особенно при хронической боли или диабете пациентов просили вести ежедневные записи), дозаторы-пилюльницы и, главное, блистеры с маркировкой дней недели. Именно в 1960-е годы была изобретена и внедрена в массовое производство блистерная упаковка, первоначально — для оральных контрацептивов. Целью этой инновации прямо заявлялось повышение удобства и приверженности: раздельные ячейки по дням позволяли женщине легко отследить, приняла ли она таблетку сегодня. В целом блистер стал первым упаковочным форматом, изначально спроектированным с учётом поведенческих аспектов — чтобы облегчить регулярный приём и избежать пропусков.

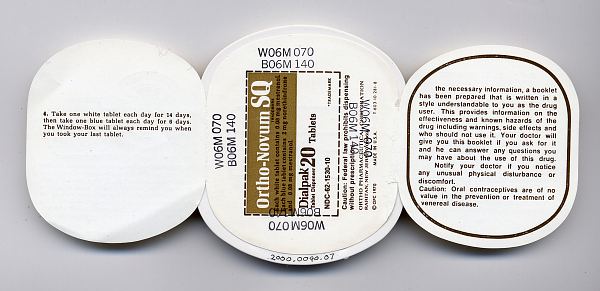
Первая блистерная упаковка Ortho-Novum SQ (Ortho, 1963 г.)
Одновременно распространяются и более простые приборы: например, карманные дозаторы и коробочки с отделениями по дням недели, которые пациент заполнял каждую неделю, раскладывая таблетки по дням.
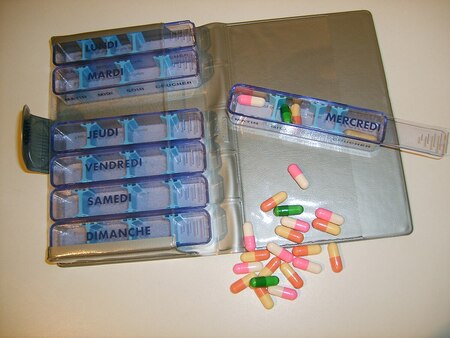

Слева: органайзер на неделю, Франция, 1960-е. Справа: органайзер «Dosett», Швеция, 1966 г.
Социальный фактор этого периода — постепенное нормирование идеи, что пациент сам отвечает за ежедневный учёт. Появляется образ «добросовестного хроника», который ставит крестики или галочки в таблице при каждом приёме лекарства. Подобная визуальная отметка прогресса дисциплинировала и мотивировала продолжать терапию.
Экономический фактор — массовое фабричное производство лекарств в упаковках: теперь у пациента всегда есть перед глазами количество оставшихся доз, и упаковка сама подсказывает, когда курс близится к завершению.
Политико-правовые факторы включают появление протоколов клинических исследований, требующих обязательного ведения дневников лечения и самочувствия. В 1960–70-е годы в рамках контролируемых испытаний пациентов снабжали стандартными бумажными дневниками, которые они должны были заполнять ежедневно ради участия в исследовании. Это привило навыки регулярной фиксации, по крайней мере, у части популяции. К концу 1970-х повседневное ведение записей о лечении из редкого индивидуального увлечения превращается в признанную норму в медицинских кругах — однако пока что в основном в клиническом контексте, под наблюдением врачей.
1990-е: персональные компьютеры и первые электронные напоминания. С распространением компьютеров и мобильной связи формы учёта начинают меняться. Артефакты этого периода — электронные таблицы и текстовые файлы (пользователи переносили схемы лечения в Excel или Word для удобства расчётов и распечатки для врача), цифровые календарные планеры, а также электронные будильники и таймеры. В некоторых исследованиях отмечалось, что уже в 1990-е появлялись первые сервисы рассылки СМС-сообщений с напоминаниями о приёме — особенно для пациентов с ВИЧ, туберкулёзом и другими заболеваниями, требовавшими строгого режима. Массово СМС-напоминания начали использоваться ближе к концу десятилетия, по мере того как мобильные телефоны получили широкое распространение.
Социально-культурные факторы: в офисной культуре 90-х закрепляется практика использования электронных календарей (Outlook, Lotus Notes и др.), и пациенты-“айтишники» нередко интегрировали расписание лекарств в свой рабочий календарь или делали таблицу, которую было легко обновлять и показывать врачу на визите. Экономически, доступность простых электронных устройств стимулировала самоуправление: многие могли позволить себе недорогие наручные часы с будильником и ставили сигнал на время дозы — это решало проблему забывчивости.
Интерфейсы календаря и блокнота Windows 3.0, 1990 г.
В правовом поле происходила стандартизация бланков врачебных назначений (вводятся унифицированные рецептурные бланки, листы назначений в стационарах). Пациенты, стремясь «говорить на одном языке» с медиками, иногда оформляли свои записи в похожей форме, подгоняли домашнюю таблицу под графы врачебного бланка. Ключевым событием рубежа веков можно считать появление массовых СМС-оповещений: например, в 1999 г. в Великобритании начала внедряться система напоминаний по телефону для пациентов с хроническими заболеваниями, а затем аналогичные проекты распространились и в других странах.
Сдвиг поведения в 1990-е можно охарактеризовать как окончательное размежевание функций: напоминание о приёме стало поступать отдельно (от устройства или сервиса), а запись о приёме — вестись отдельно (в тетради или файле). То есть, технология решила проблему своевременного сигнала, но не объединила сигнал с фиксацией эффекта. Эта разобщенность сохранилась и в дальнейшем: пользователь мог получить СМС или звук будильника («примите лекарство сейчас»), подтвердить приём нажатием кнопки — а вот информацию о самочувствии после, как правило, нужно было где-то записать вручную.
2000-е: веб-сообщества пациентов и популяризация PRO. В начале XXI века, с одной стороны, продолжает расти число людей с хроническими заболеваниями, требующих постоянной терапии, с другой — интернет становится доступным все более широким слоям. На этом фоне складывается культура онлайн-сообществ пациентов: появляются форумы, где люди обмениваются опытом лечения и начинают выкладывать шаблоны дневников и таблиц. Артефакты данного периода включают пользовательские шаблоны для печати (форматы в Word, PDF с таблицами для заполнения от руки), онлайн-форумы и блоги, где пациенты делились своими записями, первые специализированные веб-дневники (веб-сайты или программы, позволяющие вносить данные о симптомах и лекарствах) и всё те же SMS/E-mail сервисы напоминаний, вышедшие на новый уровень. К середине 2000-х концепция Patient-Reported Outcomes (ПРО, пациент-сообщаемых исходов) становится частью официальных рекомендаций FDA и EMA, о чём говорилось выше. Однако на бытовом уровне она проявляется фрагментарно: пациенты перенимают из клинической сферы отдельные инструменты — например, начинают использовать шкалы боли и настроения в своих записях (визуально-аналоговые шкалы, рейтинги от 1 до 5 и т. п.), но делают это выборочно и без привязки к конкретному приёму лекарства.
Социальный фактор этого времени — формирование коллективных эталонов самоотчёта: на форумах люди публикуют примеры идеальных дневников («как вести дневник головной боли»), происходит своеобразное самообучение. Появляются общественные инициативы по ведению дневников, например, дневники питания при диабете или астмы, которые пользователи берут из открытых источников. Экономический фактор — многими онлайн-инструментами можно было пользоваться бесплатно; к тому же сами компьютеры и интернет к 2000-м стали существенно доступнее, что сняло финансовый барьер для электронного учёта.
Правовой и институциональный фактор — доклады ВОЗ о приверженности терапии (2003 г.) и первые гайдлайны регуляторов по использованию PRO (конец 2000-х) привлекли внимание медсообщества к проблеме фиксирования данных. Однако в практику лечения это внедрялось медленно: пациенты слышали о «необходимости вести дневник» скорее от других пациентов, чем от врачей. Ключевыми событиями периода можно считать публикацию отчёта ВОЗ «Adherence to long-term therapies: Evidence for action» (2003), где подчёркивалась важность учёта принимаемых препаратов и объективных исходов, а также выход руководств FDA по PRO (например, 2009 г., руководство по применению PRO в клинических исследованиях).
Сдвиг поведения: язык самоотчёта обогащается — пациенты начинают описывать своё состояние более формально (вводят оценки, упоминают конкретные показатели), но связь «приём лекарства — последующий эффект» по-прежнему выстраивается вручную. В бытовых записях лекарства и самочувствие фигурируют, но пользователь сам должен сопоставить: «вот здесь я принял дозу, а через несколько часов у меня поднялась температура». Никакой автоматической сцепки данных в то время не существовало.
2010-е: эпоха смартфонов, платформ здоровья и носимых датчиков. В течение 2010-х произошла цифровая революция в персональном учёте здоровья. Артефакты этого периода — повсеместно распространённые мобильные приложения для напоминаний и трекинга, экосистемы наподобие Apple HealthKit и Google Fit (запущены в 2014 г.), множество коммерческих трекеров активности, сна и пульса, а также новые практики вроде фотографирования блистеров (как доказательство или напоминание о приёме) и ведения записей через облачные сервисы (таблицы Google, заметки в мобильных приложениях).
Интерфейс мобильного приложения Apple Health Kit, 2014 г.
Социально в это десятилетие меняется стиль взаимодействия с врачом: появляется возможность отправить врачу данные дистанционно. Пациенты всё чаще показывают врачу скриншоты графиков из приложений или распечатки экспортированных данных, потому что это быстрее и удобнее, чем пытаться пересказать устно. Например, гипертоник может принести на приём распечатанный график своих утренних измерений давления за месяц, вместо того чтобы вручную выписывать значения. Выросшее поколение «цифровых» пациентов привносит в коммуникацию с медиками новую норму — делиться данными, собранными самостоятельно (пускай и не всегда запрошенными).
Экономически, рынок приложений здоровья в 2010-е работал по модели freemium: базовые функции (ввести напоминание, отметить приём, записать симптом) предоставляются бесплатно, но расширенные возможности — аналитика, экспорт данных, синхронизация с медицинской картой — за отдельную плату. Это привело к тому, что многие пользователи вели минимальный объём данных («только чтобы не забыть выпить таблетку»), а глубокий анализ или интеграцию данных откладывали или игнорировали. Политико-правовая среда: массовое внедрение электронных медицинских карт, электронных рецептов и интеграционных стандартов (HL7/FHIR) означает, что в принципе с 2010-х появилась техническая возможность подтягивать данные о назначениях автоматически из аптечной или врачебной системы. Некоторые приложения начали реализовывать функциональность загрузки списка препаратов по электронному рецепту или через доступ к медкарте. Однако связывание этих данных с пользовательскими записями о симптомах осталось слабым звеном. То есть приложение могло знать, что «пациенту выписано лекарство X, 2 раза в день», но автоматом сопоставить с ежедневником головной боли эту информацию было сложно — слишком разнородные данные.
Ключевое событие периода — запуск крупными игроками своих платформ mHealth: Apple в 2014 г. интегрировала приложение «Здоровье» (Health) в iOS с возможностью сторонним приложениям записывать туда данные, Google в том же году представила Google Fit с похожей идеей централизации фитнес и медданных. Это создало инфраструктуру для объединения данных о физической активности, параметрах тела и даже о приёмах лекарств в одном месте (при условии, что приложения будут синхронизироваться).
Сдвиг поведения пользователей в 2010-е можно охарактеризовать как консолидацию инструментов: напоминания и записи теперь находятся на одном устройстве — смартфоне, который всегда под рукой. Однако нередко они все еще разнесены по разным приложениям или экранам. Например, напоминание всплывает в пуш-уведомлении, а чтобы сделать запись о самочувствии, нужно открыть другое приложение и ввести там данные. Пользователь по-прежнему выполняет роль «моста», вручную перекладывая контекст между двумя потоками информации. Тем не менее, в массовом сознании укрепляется ожидание, что «в телефоне должно всё храниться» — то есть люди уже начинают систематически вести цифровой журнал здоровья, хотя бы и разрозненный.
2020-е: телемедицина, электронные рецепты и удалённый мониторинг. Наконец, самое последнее десятилетие (начало 2020-х) ознаменовалось резким ростом дистанционных способов ведения и использования данных о лечении. Артефакты этого времени — это, во-первых, средства удалённого общения с врачом: видеоконсультации, защищённые чаты между пациентом и доктором. Во-вторых, полноценные электронные рецепты практически полностью заменили бумажные в ряде стран, а вместе с ними — и интеграция с аптечными системами: теперь пациент может видеть список своих текущих препаратов в личном кабинете больничной системы или приложения страховой. В-третьих, широкое распространение получили домашние медицинские приборы с функцией автозаписи — от тонометров и глюкометров, передающих данные врачу через интернет, до «умных» пилюльниц и сенсорных крышек для бутылочек с таблетками, которые фиксируют факт открытия и тем самым — приём дозы. Например, существуют гаджеты, которые отправляют сигнал в приложение при каждом вытаскивании таблетки из ячейки блистера либо при открытии контейнера, автоматически отмечая дату и время события.
Социальные факторы этого периода связаны, во многом, с пандемией COVID-19: в 2020 г. локдауны заставили множество пациентов и врачей перейти на удалённые консультации. Если раньше некоторые пациенты приходили на приём с тетрадью, то при видеосвязи врач мог попросить: «вышлите мне перед встречей данные за последнюю неделю». В итоге люди начали заранее заполнять дневник перед телеприёмом — чтобы быть готовыми озвучить конкретные цифры или переслать файл. В онлайне пациент часто ощущает большую ответственность за предоставление данных, ведь врач «на том конце» видит только то, что ему покажут. Поэтому режим «поделиться фрагментом дневника под задачу» окреп: например, за 3 дня до планового видеоприёма эндокринолог может попросить выслать дневник сахаров и инсулинов, и пациент формирует из своего трекера отчёт ровно за нужный период.
Экономический фактор: здравоохранение всё активнее стимулирует удалённый мониторинг — в некоторых системах страховые компании и клиники получают возмещение за услугу удалённого наблюдения, если обеспечат сбор определённых данных. В США, например, с 2020 г. Medicare и частичные Medicaid стали оплачивать программы Remote Patient Monitoring (RPM) по специальным CPT-кодам. Для этого требуются формализованные шаблоны: как минимум 16 измерений в месяц, автоматически переданных от прибора, или фиксированное количество минут, которое медработник анализирует данные. В результате в некоторых случаях пациента фактически обеспечивают готовыми устройствами и инструкциями, что и когда измерять и заносить, чтобы выполнились критерии.
Правовая среда начала 2020-х продолжает линию тотальной цифровизации: электронные медицинские обмены (форматы HL7/FHIR) стали обязательными для совместимости систем, рецепты и врачебные назначения — машиночитаемыми, а обмен данными между устройствами — защищённым стандартами (например, протоколы Bluetooth для медтехники, профили IEEE для глюкометров и пр.). Тем не менее, даже при этой технической связанности, смысловую связность «доза — эффект» системы по-прежнему не обеспечивают автоматически. Связать информацию о принятом препарате и показания домашнего пульсометра через 2 часа — задача или самого пациента, или его врача (не всегда очевидно, что именно нужно сопоставить).
Ключевое событие периода — глобальный переход амбулаторных приёмов в онлайн-режим в 2020–2021 гг. и закрепление этого на нормативном уровне (например, в ряде стран узаконены телемедицинские консультации, дистанционное продление рецептов и пр.). Сдвиг поведения: к 2025 г. параллельный учёт (приёмы и симптомы) фактически стал ожидаемой нормой — пациента заранее спрашивают, ведёт ли он какие-то записи о своём состоянии. Однако полностью устранить разрывы данных не удалось: «мост» между двумя потоками (лекарства и самочувствие) по-прежнему строит сам пользователь, комбинируя разные цифровые и аналоговые средства. Это приводит нас к аналитической оценке и выводам.
Анализ исторических и современных практик позволяет выделить повторяющиеся точки распада связки «приём препарата — самочувствие». Во-первых, это разрыв во времени фиксации: приём отмечается сразу, симптомы — позже, либо наоборот. Во-вторых, это разрыв в языке описания: приём фиксируется формально (доза, время), самочувствие — качественно и эмоционально, без шкал и сопоставимых единиц. В-третьих, это разрыв в адресате: записи ведутся с разной предполагаемой аудиторией, что меняет степень откровенности и точности. В-четвёртых, это разрыв в контексте: симптомы фиксируются без учёта сна, питания, стресса, что делает связь с препаратом неоднозначной. Наконец, это разрыв в ответственности: система хранит данные, но не «отвечает» за их связность, перекладывая работу интерпретации на пользователя. Эти точки распада устойчиво воспроизводятся независимо от технологического уровня и потому требуют не локальных улучшений интерфейса, а пересмотра самой единицы учёта.
Аналитический обзор и выводы
Проследив исторический путь, мы видим, что переход от офлайн к онлайн инструментам практически не изменил базовой социальной логики: люди по-прежнему ведут учёт ради двух целей — (1) напомнить себе принять лекарство и (2) отчитаться врачу о результатах. Цифровые технологии унаследовали эту двойственность и даже укрепили её, предоставив усовершенствованные средства напоминания (звуковые сигналы, уведомления) и облегчив обмен данными (файлы, скриншоты, синхронизация).
Однако автоматического замыкания причинно-следственной связки между параллельными потоками данных не случилось. Как и десятилетия назад, последовательность «принял дозу — ощутил эффект — записал это» требует активных действий и внимания от пациента. Систематические разрывы (не записал эффект, не указал время приёма, забыл внести изменение дозы и т. п.) по-прежнему возникают, пусть и в новых формах. Это снижает качество данных и ведёт к описанным рискам лечения. Тем не менее, анализ позволяет наметить мегатренды, формирующиеся в ответ на эти проблемы. Ниже выделены три главных направления (мегатренда), которые определяют развитие инструментов учёта «препарат ↔ состояние» в ближайшем будущем.
Институциональные и региональные различия
На первый взгляд может показаться, что распад связки «приём препарата — самочувствие» является следствием недостаточной цифровизации и потому должен исчезать в системах здравоохранения с развитой инфраструктурой электронных рецептов, медицинских карт и телемедицины. Однако сравнительный анализ практик в разных институциональных контекстах показывает обратное: даже при высоком уровне технологической зрелости разрыв сохраняется, меняя лишь форму проявления. Это указывает на то, что причина лежит не столько в доступности технологий, сколько в распределении ролей, ответственности и смыслов между пациентом, врачом и системой.
В системах здравоохранения стран Западной Европы ключевым фактором является институциональная ориентация на стандартизацию и доказательность. Электронные рецепты, централизованные реестры лекарств и формализованные протоколы наблюдения обеспечивают высокую структурированность данных о назначениях. Пациент, как правило, имеет доступ к списку препаратов, дозировок и дат, а иногда и к напоминаниям, встроенным в национальные порталы. Однако фиксация самочувствия в этих системах чаще остаётся эпизодической и «привязанной к событию контакта» — визиту или исследованию. Причина в том, что вне клинического контекста система не предъявляет устойчивого запроса на данные о субъективном состоянии. В результате пациент ведёт дневник либо для себя, либо по требованию врача, но не как постоянную часть инфраструктуры лечения. Связка «приём — эффект» возникает только в моменты формализованного взаимодействия, а не в повседневности.
В США ситуация иная по устройству, но сходна по результату. Здесь большую роль играет рыночная и страховая логика. Электронные рецепты и приложения для приёма лекарств широко распространены, однако цифровые сервисы часто ориентированы либо на соблюдение схемы (adherence tracking), либо на сбор данных для отчётности и биллинга. Пациент оказывается в системе, где данные ценятся постольку, поскольку они могут быть использованы для принятия административных решений: подтверждения услуги, корректировки покрытия, участия в программах мониторинга. Самочувствие при этом фиксируется через стандартизированные PRO-инструменты, но чаще в рамках конкретных программ или исследований. В повседневной жизни пользователь сталкивается с множеством разрозненных приложений, каждое из которых оптимизировано под свою метрику. Это усиливает фрагментацию и переводит работу по интерпретации на самого человека: он должен собрать данные из разных источников, чтобы понять, как именно лечение влияет на его состояние
В российском контексте и ряде постсоветских систем ключевым фактором становится асимметрия формализации. Электронные рецепты и медицинские карты внедряются неравномерно, а значительная часть лечения продолжает существовать в гибридном режиме: часть данных формализована, часть остаётся в устной или неструктурированной форме. Это усиливает роль пациента как «сборщика информации»: он одновременно хранит бумажные назначения, переписывает схемы в заметки, ведёт собственные таблицы и фиксирует самочувствие в произвольном виде. Здесь разрыв связки усугубляется отсутствием единого стандарта взаимодействия: врач может ожидать структурированного отчёта, но не предоставлять инструмента для его ведения. В результате дневник становится персональным изобретением, а не частью системы.
Несмотря на различия, во всех этих контекстах воспроизводится одна и та же логика: система здравоохранения хорошо умеет работать с объектами (препаратами, дозами, назначениями), но плохо — с отношениями между объектами и переживаемыми эффектами. Институционально эффект терапии по-прежнему считается областью клинической интерпретации, а не предметом повседневного учёта. Это означает, что пациенту не предлагается устойчивый формат для фиксации именно связи «принял — почувствовал», поскольку сама система не признаёт эту связку самостоятельной сущностью данных.
Дополнительным фактором становится различие в ожиданиях от роли пациента. В системах с сильной ориентацией на автономию пациенту делегируется ответственность за самоменеджмент, но не предоставляется соответствующая когнитивная поддержка. В системах с более патерналистской традицией пациент ожидает, что интерпретация будет сделана врачом, и потому не инвестирует усилия в систематическую фиксацию эффекта. В обоих случаях возникает вакуум: либо данные есть, но не осмыслены, либо ожидание осмысления блокирует сбор данных.
Таким образом, региональные различия показывают, что цифровая зрелость сама по себе не решает проблему связки «приём — самочувствие». Напротив, чем сложнее и насыщеннее инфраструктура, тем выше риск фрагментации, если отсутствует слой, специально предназначенный для удержания причинных отношений. Это усиливает тезис о том, что разрыв является не временным этапом эволюции, а системным эффектом того, как медицинские данные исторически разделены на «назначения» и «исходы».
Этот слой анализа принципиально важен, поскольку он позволяет обосновать универсальность проблемы и избежать локального объяснения через особенности конкретного рынка. Продуктовая концепция, ориентированная на удержание связки «препарат — самочувствие», встраивается не как локальное улучшение интерфейса, а как ответ на структурный дефицит, присутствующий в разных институциональных моделях здравоохранения.
Эпистемологический слой: почему знание о лечении изначально разделяет «приём» и «самочувствие»
Распад связки «приём препарата — самочувствие» имеет не только исторические, технологические или институциональные причины, но и более глубокое эпистемологическое основание. Он укоренён в том, каким образом медицинское знание в целом организует и легитимирует разные типы данных. В классической биомедицинской парадигме воздействие и переживание принадлежат разным режимам знания: первое относится к области объективируемых действий и веществ, второе — к области субъективного опыта, который допускается к учёту лишь при соблюдении специальных условий.
Фармакологическое знание строится вокруг вещества, дозы, механизма действия и воспроизводимого эффекта на уровне популяции. Препарат существует как объект, чьи свойства считаются независимыми от конкретного пациента, а различия между людьми трактуются как вариации вокруг нормы. Именно поэтому приём препарата легко превращается в структурируемую сущность: его можно описать формулой, дозировкой, временем, частотой. Эти параметры хорошо поддаются стандартизации, автоматизации и передаче между системами. В эпистемологическом смысле приём — это «жёсткий факт», который либо произошёл, либо нет, и потому идеально подходит для учёта.
Самочувствие, напротив, относится к другому типу знания. Оно не существует как внешний объект и не обладает однозначной шкалой измерения. Симптомы переживаются во времени, зависят от контекста и языка описания, меняются в зависимости от ожиданий, тревоги, прошлого опыта и социальных норм. Исторически медицина относилась к этому типу знания с осторожностью: субъективные ощущения считались ненадёжными, склонными к искажению и требующими перевода в клинически допустимую форму. Именно поэтому самочувствие допускалось в медицинское знание через фильтры — шкалы, опросники, стандартизированные формулировки. До прохождения такого перевода оно оставалось «неполноценным» знанием.
Это фундаментальное различие привело к асимметрии статуса данных. Данные о приёме лекарства считаются первичными и валидными по умолчанию, тогда как данные о самочувствии — вторичными и требующими подтверждения. Даже когда медицина признаёт важность пациентского опыта (через PRO и ePRO), он включается в систему как отдельный слой, подчинённый правилам клинической валидации. В результате связь между приёмом и переживаемым эффектом не мыслится как самостоятельная единица знания. Она всегда реконструируется постфактум — через анализ, интерпретацию, корреляции, — но не фиксируется как базовая сущность.
Эта эпистемологическая установка напрямую отражается в инструментах фиксации. Дневники лечения, как правило, повторяют логику науки: они отдельно спрашивают «что вы приняли» и отдельно — «что вы почувствовали». Связь между этими ответами предполагается, но не задаётся структурно. Пользователь должен сам выполнить работу синтеза, которая в научной практике делегируется исследователю или врачу. Таким образом, пациент оказывается в позиции «непрофессионального аналитика», которому предлагают сырые данные без инструментов для удержания причинности.
Важно подчеркнуть, что даже цифровизация и рост вычислительных возможностей не устраняют эту проблему автоматически. Напротив, цифровые системы часто усиливают эпистемологическое разделение, поскольку они особенно хорошо работают с формализуемыми объектами и хуже — с контекстуальным, многозначным опытом. Алгоритмы требуют чётких полей, единиц измерения и временных меток; субъективное самочувствие же сопротивляется такому формату и потому либо упрощается до формальных шкал, либо вытесняется в свободный текст и заметки. В обоих случаях причинная связка оказывается ослабленной: либо из-за потери нюансов, либо из-за невозможности машинной обработки.
Дополнительное напряжение создаёт временное расхождение режимов знания. Приём препарата — моментальное событие, которое легко зафиксировать во времени. Эффект же может быть отсроченным, накопительным или нестабильным. Эпистемологически медицина привыкла работать с усреднёнными временными окнами («через столько-то часов», «через столько-то дней»), тогда как пациент живёт в режиме непрерывного наблюдения и неопределённости. Отсутствие согласованного временного языка для описания эффекта приводит к тому, что связь либо упрощается до линейной («принял — стало лучше/хуже»), либо вовсе распадается.
Таким образом, распад связки «приём препарата — самочувствие» можно рассматривать как следствие глубинного разделения типов знания: объективируемого действия и субъективного переживания. Инструменты учёта наследуют эту дихотомию и воспроизводят её на уровне интерфейсов и сценариев использования. Пользователь оказывается между двумя эпистемологическими режимами, не имея средства удерживать их в едином контуре.
Этот вывод позволяет сформулировать новизну не как «улучшение дневника» или «интеграцию данных», а как попытку эпистемологического сдвига: признание связки «принято — почувствовано» самостоятельной единицей знания, которая должна быть зафиксирована и визуализирована напрямую, а не реконструирована задним числом. Такой подход предполагает проектирование интерфейсов, где событие приёма автоматически инициирует наблюдение за эффектом, а субъективный опыт получает статус первичного сигнала, а не вторичного комментария. Тем самым визуальное и продуктовое решение становится не просто удобным инструментом, а способом переосмыслить, как именно знание о лечении может быть собрано, удержано и использовано в повседневной практике.
Мегатренды
Мегатренд 1: Causal Self-Logging (причинно-ориентированный самотрекинг). Пользователи всё более ожидают от своих записей не просто накопления данных, а выявления и отражения причинно-следственных пар. Иными словами, вместо разрозненных списков «что приняли» и «как чувствовали себя» возникает требование связывать эти факты: какую дозу принял — что после этого почувствовал — через сколько времени. В массовую практику входят точные временные метки и оценки состояния через короткие интервалы после приёма. Например, приложения теперь предлагают ввести не только факт приёма лекарства, но и через час ответить на вопрос о самочувствии (оценить боль по шкале, уровень симптома). Нормой становится сопровождать запись о симптоме контекстом — указывая, что могло повлиять (например, «головная боль 5/10, спустя ~2 часа после таблетки, возможно из-за недосыпа»).
Такие связки востребованы как самими пациентами, стремящимися понять эффективность терапии, так и врачами и страховщиками, которые хотят получать осмысленные данные, а не сырые логи. Появляется понятие индивидуального N-of-1 эксперимента: некоторые пациенты подходят к самонаблюдению почти научно, фиксируя причинно-следственные гипотезы (например, что будет с давлением, если сдвинуть время вечернего приёма лекарства) и проверяя их в своих данных. В целом тренд направлен на то, чтобы дневники перестали быть пассивным хранилищем и превратились в инструмент саморегуляции через обратную связь. Это ведёт к усложнению модели данных (нужно хранить связи «доза–реакция»), но обещает новую ценность — персонализированную причинную аналитику.
Мегатренд 2: Accountable Sharing (адресное и контролируемое деление данными). Второй важный тренд — укрепление режима частичного, ролевого обмена данными о лечении. Если раньше дневник был либо полностью личным, либо целиком показывался врачу, то теперь все чаще практикуется селективное шаринг: поделиться нужным фрагментом с нужным человеком под конкретную задачу. Например, члены семьи получают доступ только к информации о соблюдении расписания (чтобы напомнить или помочь, но без деталей симптомов, которые пациент предпочитает не раскрывать). Для врача, напротив, готовится краткая сводка по существенным параметрам за последние, скажем, 7–14 дней — и больше он не увидит. Технологически это стало проще: современные платформы (включая решения от крупных компаний) вводят функции, позволяющие пользователю самому выбирать, какие именно данные из Health-дневника открыть для просмотра тому или иному адресату.
В iOS, к примеру, с 2021 года реализован модуль Health Sharing: пользователь может отметить галочками, что он делится с врачом только показателями пульса и количеством шагов, а с дочерью — еще и оповещениями о падениях и параметрами сна. Культура взаимоотношений вокруг данных тоже меняется: обмен становится условием получения помощи и качественной услуги. Пациент уже понимает, что врачу удобнее просмотреть реальную динамику, чем услышать субъективный рассказ. В то же время сохраняется обеспокоенность приватностью — и ответом на неё как раз служат механизмы ограниченного доступа (по времени и по содержанию).
Можно говорить о формировании нового социального контракта: пациент готов более ответственно и открыто вести дневник и делиться им, но взамен ожидает контроля над своими данными и уважения границ. Для проектов параллельного учёта это означает необходимость встроить гибкие настройки доступа и экспорта (например, отдельные режимы «для врача», «для семьи», «для личного пользования»). Подобная концепция уже легла в основу ряда инициатив: так, в Европе обсуждаются стандарты разделения медицинских записей на зоны видимости, а в США Apple Health позволяет отдавать данные напрямую в медицинскую систему врача при подтверждении согласия. Можно прогнозировать, что в ближайшие годы «accountability» (отчётность) дневников возрастёт — т. е. они будут все чаще выступать как официальный источник информации для разных заинтересованных сторон, от врача до страховой, — но при этом пользователь сохранит роль управления, решая, кто и что увидит.
Мегатренд 3: Ambient Adherence (встроенная, окружающая приверженность). Третий мегатренд связан с проникновением технологий Интернета вещей и искусственного интеллекта в повседневную среду пациента. Идея заключается в том, чтобы максимальная часть учёта выполнялась без активных действий пользователя, за счёт возможностей окружающих его устройств и сенсоров. Уже сейчас наручные фитнес-браслеты автоматически измеряют пульс, распознают фазы сна и передают эти данные в телефон. «Умные» колонки могут по голосовой команде напомнить о лекарствах.
Следующий шаг — автоматическое фиксирование самого факта приёма препарата. Существующие разработки включают, например, сенсорные крышки для бутылочек, фиксирующие открытие (решение типа MEMS Cap от AARDEX), смарт-блистеры с микроцепями, посылающими сигнал при нажатии на ячейку, а также экспериментальные методы вроде распознавания жестов глотания через носимые датчики. Появляются и системы компьютерного зрения, способные определить, что человек взял лекарство из упаковки (например, камера на кухне, анализирующая движение руки к органайзеру). Такой «рассеянный» сбор данных ведёт к тому, что система сама знает время и дозу приёма — и может автоматически сопоставить с другими контекстными данными (пульс, давление, уровень активности). Ожидание пользователей формируется соответствующее: «пусть всё записывается само, а я только подтвержу и прокомментирую».
Ambient Adherence как paradigma означает, что соблюдение режима и его регистрация становятся частью окружения. Это снимает когнитивную нагрузку (не надо помнить и вручную отмечать), но предъявляет требования к интеграции устройств. В проектировании будущего приложения этот тренд учитывается как направление развития: возможность подключить по API умный тонометр или трекер, импортировать данные из аптечной системы о выданных рецептах и пр. — всё это позволит приблизиться к идеалу, когда минимум ручных действий при максимуме связности данных.
Конечно, такие технологии порождают и новые вызовы — от технических сбоев до вопросов конфиденциальности — но общая тенденция очевидна. Рынок уже предлагает множество «умных» решений для повышения приверженности (smart pill boxes, датчики и напоминания), и их сочетание с программными платформами даст эффект практически незаметного для пациента сбора данных, из которых затем можно строить понятные ему же причинно-следственные цепочки.
Трендвотчинг исследование
Без систематического контроля пациенты не всегда связывают изменения самочувствия с приёмом лекарства: эффект может быть отсроченным или скрытым другими факторами, и причинно-следственная связь «препарат — самочувствие» нередко распадается. Современные цифровые решения стремятся эту связь удержать: сформировались новые подходы — ведение дневников здоровья, социальная поддержка и умные «фоновые» напоминания — которые помогают пациенту осознавать влияние терапии на своё состояние.
Одной из ключевых тенденций стала практика персонализированного самонаблюдения за здоровьем. Пациенты всё чаще ведут дневники или используют мобильные приложения для фиксации фактов приёма лекарств и симптомов, стремясь выявить причинно-следственные зависимости между лечением и самочувствием. По оценкам, порядка двух третей взрослых практикуют такой самоконтроль, и исследования подтверждают, что регулярный сбор собственных данных способен существенно улучшать управление здоровьем. Накопленные таким образом данные делают влияние терапии более очевидным для пациента, помогая ему дисциплинированнее соблюдать назначения врача.
Социальное окружение тоже играет важную роль. Исследования показывают, что наличие поддержки достоверно связано с более высоким соблюдением режима терапии. На практике применяются разные стратегии: от договорённостей с близкими о регулярных напоминаниях до публичного обмена успехами лечения в онлайн-сообществах. Цифровые сервисы создают для этого специальные платформы, а представители отрасли отмечают «силу социальной поддержки и разделённого опыта» пациентов. Вовлечение других людей делает лечение более прозрачным для пациента и формирует дополнительную мотивацию придерживаться курса.
Кроме того, заметна тенденция внедрения технологий, интегрирующих поддержку приверженности терапии в повседневную среду. Современные устройства способны действовать почти незаметно, обеспечивая контроль и напоминания в фоновом режиме. Уже существуют решения, делающие приём лекарств максимально удобным и исключающим случайные пропуски: от интерактивных уведомлений на смартфоне до интеллектуальных контейнеров для таблеток и носимых сенсоров. Например, «умный» флакон может световым сигналом и автоматическим сообщением напомнить о дозе и даже предупредить близких о пропуске. Таким образом, технологии Интернета вещей превращают окружение пациента в незримого помощника, незаметно следящего за соблюдением терапии
Совокупность этих трендов подчёркивает актуальность создания интегрированного решения для одновременного учёта приёма препаратов и динамики самочувствия. Пользователи ожидают, что цифровые инструменты будут не только напоминать о лекарствах, но и отслеживать показатели благополучия, анализировать их и позволять делиться прогрессом. Поэтому разработка специального мобильного приложения представляется логичным шагом, отвечающим на выявленные запросы. Такое решение объединит элементы всех обозначенных подходов: персональное журналирование, социальную поддержку и автоматизированные напоминания. Это обеспечит непрерывную обратную связь между лечением и ощущениями пациента, повышая его осознанность и приверженность терапии. Далее в работе описывается данное продуктовое решение.
Заключение
Визуальное исследование, проведённое автором позволило выявить новые аспекты проблемы учёта принимаемых препаратов и состояния здоровья. В теоретическом плане оно показало междисциплинарную природу задачи: успешное решение требует учёта поведенческих, когнитивных, социальных и технологических факторов. Практическая значимость результатов заключается в том, что сделанные наблюдения напрямую информируют дипломный проект — приложение для параллельного учёта. В частности, концепция приложения будет опираться на выявленные мегатренды: реализует привязку записи самочувствия к конкретным дозам (causal logging), внедрит режимы выборочного шеринга данных под разные нужды (accountable sharing) и заложит интеграцию с умными устройствами для автоматизации части учёта (ambient adherence). Практически, полученные наблюдения лягут в основу дизайн-решений дипломного проекта: приложение будет разрабатываться с учётом исторически сложившихся пользовательских привычек и барьеров, чтобы предложить новаторское, но жизнеспособное решение проблемы распадающихся данных о лечении.



